Research

心血管疾患の運動療法、スポーツ
日本人の死亡原因の第2位は心疾患(15.5%)であり、両者で全体の1/4を占めています。(厚生労働省「平成23年人口動態統計」)。そのため、心血管疾患に対する費用対効果の高い診断法、治療法の提供は、医療財源を圧迫することなく国民の健康寿命を延長するためにとても重要です。心血管イベントの予防には、栄養療法や運動療法などの早期介入が重要となる。ACC/AHA (米国心臓病学会/米国循環器学会)「心血管疾患リスク低減のための生活習慣マネジメントのガイドライン」では、脳心血管疾患の強いリスク因子である血清コレステロールおよび血圧を低下させるために、有酸素運動を40分間、週3-4回実施することが推奨されており、心血管疾患に対する運動療法の有効性は広く認められているところです (Ann Int Med 2005 143 659-, JAMA. 2009;301(14):1451, JACC 2012;60:1521-)。現在、医療機関において、医療者が日常生活での適切な運動強度(多くの心血管疾患は有酸素運動レベル)を指導していますが、実際の日常生活の中で、適切な運動強度が守られている例は希で、効率が低いだけでなく過剰な負荷によって心血管イベントを誘発する危険があります。また、医療者が、患者の活動レベルを患者の状態に合わせて、客観的に把握することは困難でした。この点が、臨床におけるジレンマであり、毎日の体調に合わせて、リアルタイムに適切な運動強度を提供し、それを医療者と共有し、リアルタイムにフィードバックするプログラムの開発は喫緊の課題となっています。
臨床
慶應義塾大学病院の2号館3階で、運動療法外来を行っています。数十年の循環器救急治療の進歩により、心筋梗塞をはじめとする虚血性心疾患の急性期死亡率は格段に減少したが、遠隔期に心不全による再入院・死亡が増加していることが問題となっています。特に、心不全患者は高齢者であることが多く、心不全の全死亡率(20%/年)や再入院率(30%/年)は近年においても大きな改善は認められていません。長期的な心不全管理では、運動トレーニングや心臓リハビリテーションの継続が重要と考えられており、その入り口である、心肺運動負荷検査を実施しています。本検査は、密着型マスクを装着しながら、運動をしていただき、運動中の呼気の酸素や二酸化炭素濃度を測定することで、運動レベルや、有酸素運動の指標である嫌気性代謝閾値を求めます。この閾値を指標に、運動を継続することで、心不全の予後や生活の質が改善することが報告されています。
また、慶應義塾大学病院内に、自費診療部門として、メディカルフィットネスセンターを開始しました。医師とトレーナーが密に連携し、医学的および科学的に適切な運動療法を提供します。科学的根拠に基づく未来型運動療法/ヘルスケアの提供を目指し、病気が発症する前(未病)の皆様に加え、病気が発症後(後病)の患者さんに対しても医療保険の適応外となっている運動だけでなく食事(食品)に関するサービスも提供します。高齢者から子供まですべての年代に、運動/食事/こころ/睡眠を最新のテクノロジーを用いてアプローチし、より健康な状態を保つサービスを展開します。
場所
慶應義塾大学病院 2号館3階 3R外来
慶應義塾大学病院 3号館3階 Sports Medical Fitness Center
研究
①健康寿命の延伸に向けた新たなフィットネス法の開発 –心臓自律神経反射機能のフィットネスへの応用-
心臓自律神経反射機能(有機的な交感神経系ならびに副交感神経系の調節)は、日常活動時の心機能の調整に関与するほか、様々な心疾患においてその発生、病態、治療、予後に密接に関係しています。特に、生命に直接影響を及ぼす心室頻拍や心室細動をはじめとした多くの不整脈は、心臓自律神経反射機能と強い関連があることが報告されています。そのため、心臓自律神経反射機能に注目した、心疾患に対する治療法の開発は喫緊の課題となっています。
脳卒中や心筋梗塞などの脳心血管イベントを予防するためには、早期診断に加え、適切な栄養や運動などを行うことが重要となります。ACC/AHA (米国心臓病学会/米国循環器学会)「心血管疾患リスク低減のための生活習慣マネジメントのガイドライン」では、血清コレステロールおよび血圧を低下させるために、有酸素運動を40分間、週3-4回実施することを推奨しています。また、脳心疾患に対する有酸素運動療法はその有効性が多く報告されています。しかし、医療機関以外で有酸素運動 (自宅やジムなどでの運動) を行う際は、脈拍数、エルゴメーターの負荷量、ボルグスケールなどを指標としますが、予想外に弱いまたは強い運動を行っている可能性があります。
我々は、2014年より最大エントロピー法を用いて漸増運動負荷中の心臓自律神経反射機能を画像化(可視化)する研究を開始しました。これまでの心拍変動解析によく使用されていたホルター心電図等ではR波の信号を125Hzで採取しており、解像度が粗いため、心拍数が150~200bpmまで上昇する運動時では心拍変動を正確に把握することが困難でした。そこで、R波の信号を1000Hzの精度で採取する技術を開発し、そのもとで最大エントロピー法を用いて、30秒間の心拍変動を1拍ごとずらしながら、漸増運動負荷中のHF, LF, L/Hを連続的に解析し、瞬時に画像化することに成功しました(図1:運動中の連続心拍変動解析HF; 赤, L/H; 青)。さらに、健常ボランティア及び心不全患者において、心拍変動がHFからL/Hに切り替わるタイミングが、嫌気性代謝閾値と相関することを発見し、1拍ごとの連続的な心拍変動解析のみから、有酸素運動限界を予測し、適切な運動強度を提供することを可能としました。この成果を心筋梗塞患者では、2018年にJournal of American heart association誌1に、心不全患者では、2023年にJournal of Clinical Medicine誌に報告しました2。さらに、2022年に、心電図モニターを装着しながら運動を行う際に、心拍変動解析を併用すると、30分間嫌気性代謝閾値での運動を継続できることを報告しました(図2)3。心臓自律神経反射機能のモニタリングにより、個々人の日々の体調に合わせ、有酸素運動限界をリアルタイムに知らせながら運動をすることを可能とするシステムの開発を行っております。そのために、現在、スポーツ医学総合センターと循環器内科が共同で以下の臨床研究を行っております。これらの研究から、多くの研究成果が報告されています4,5,6。
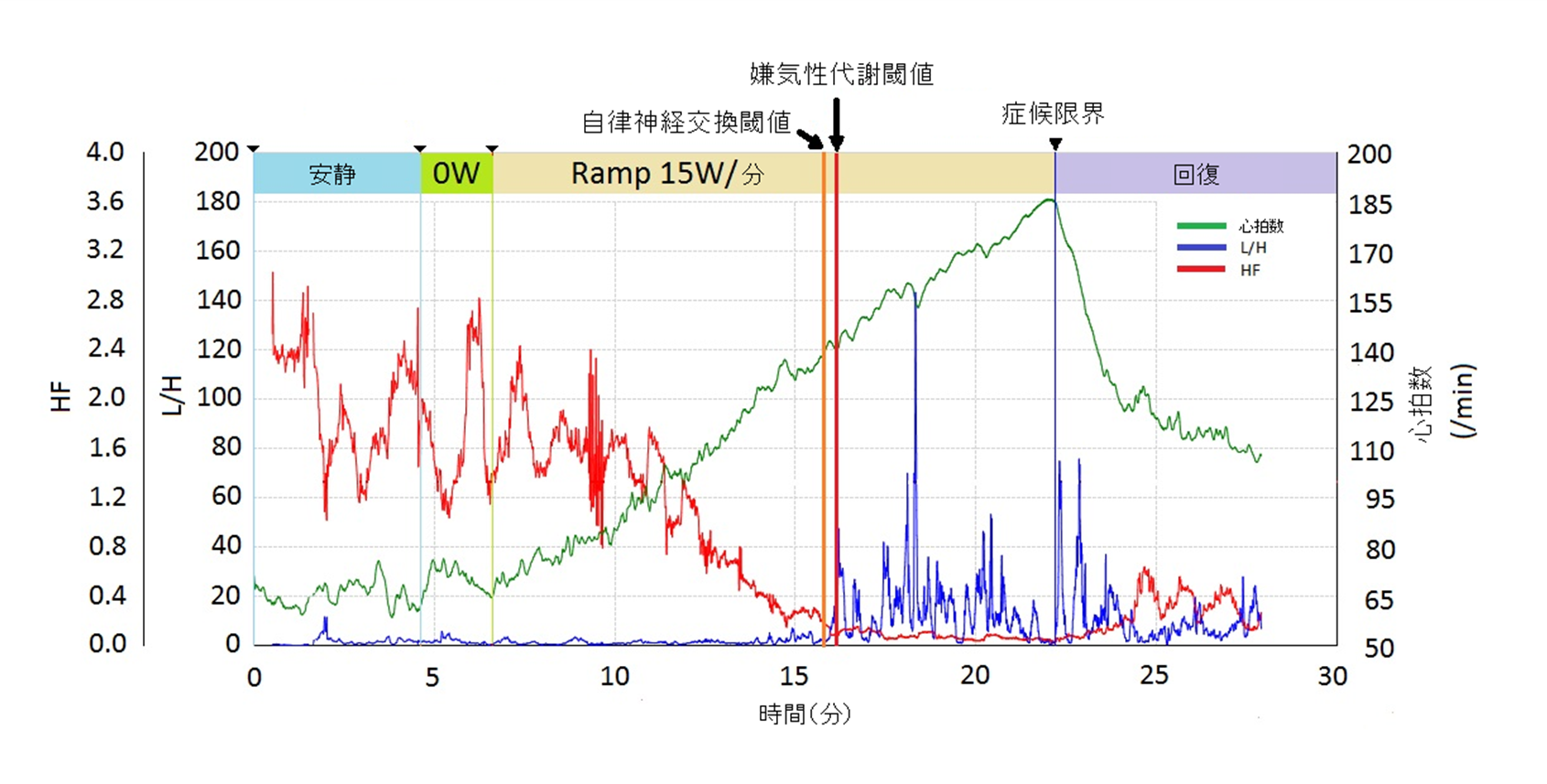
図1
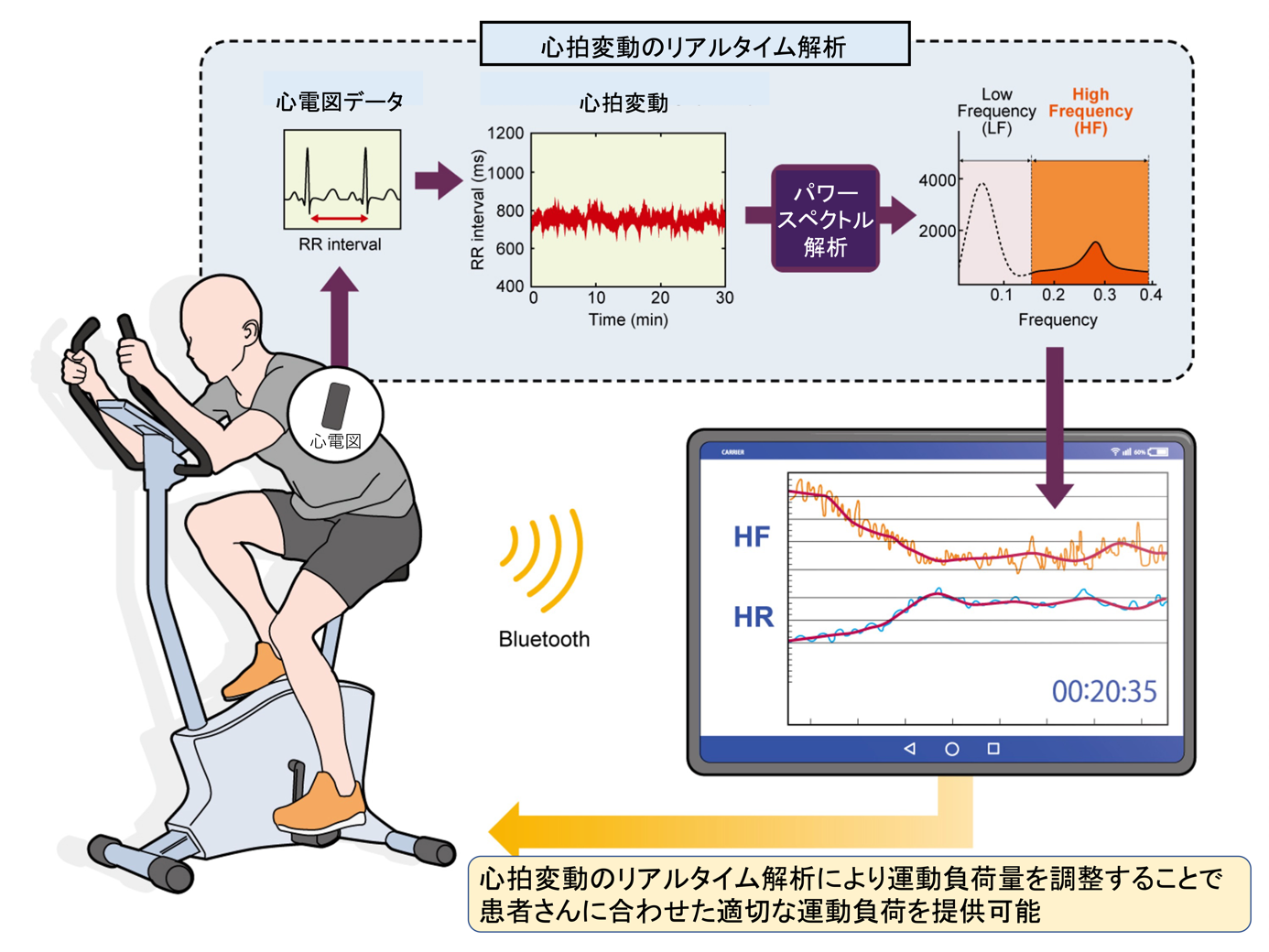
図2
主な研究
心血管疾患と自律神経活動の関連研究に関するご協力のお願い (2014年6月3日~)
運動中の非侵襲的心臓自律神経活動評価法の検証研究に対するご協力のお願い(2015年12月4日~)
関連論文
1.Shiraishi Y, Katsumata Y, et al. Real-Time Analysis of the Heart Rate Variability During Incremental Exercise for the Detection of the Ventilatory Threshold. J Am Heart Assoc. 2018 Jan 7;7(1):e006612. doi: 10.1161/JAHA.117.006612.
2.Ryuzaki T, Shiraishi Y, Miura K, Ikura H, Seki Y, Azuma K, Sato K, Fukuda K, Katsumata Y. Real-Time Estimation of Anaerobic Threshold during Exercise Using Electrocardiogram in Heart Failure Patients. J Clin Med. 2023 Aug 11;12(16):5225. doi: 10.3390/jcm12165225.
3.Ito W, Uchiyama K, Mitsuno R, Sugita E, Nakayama T, Ryuzaki T, Takahashi R, Katsumata Y, Hayashi K, Kanda T, Washida N, Sato K, Itoh H. Correlation between acylcarnitine/free carnitine ratio and cardiopulmonary exercise test parameters in patients with incident dialysis. Front Physiol. 2023 Mar 7;14:1155281. doi: 10.3389/fphys.2023.1155281.
4.Ikura H, Katsumata Y, et al. Real-time analysis of heart rate variability during aerobic exercise in patients with cardiovascular disease. Int J Cardiol Heart Vasc. 2022 Nov 11;43:101147. doi: 10.1016/j.ijcha.2022.101147.
5.Miura K, Katsumata Y, et al. Exercise tolerance and quality of life in hemodynamically partially improved patients with chronic thromboembolic pulmonary hypertension treated with balloon pulmonary angioplasty. PLoS One.2021 Jul 23;16(7):e0255180. doi: 10.1371/journal.pone.0255180.
6.Katsumata Y, et al. A high BNP level predicts an improvement in exercise tolerance after a successful catheter ablation of persistent atrial fibrillation. J Cardiovasc Electrophysiol. 2019 Nov;30(11):2283-2290. doi:10.1111/jce.14149.
②画期的なセンシングデバイスの開発:汗乳酸センサや携帯アプリの医療への応用
心血管疾患に対する運動療法の有効性は広く認められているところです。我々は運動中の乳酸値を非観血的かつリアルタイムに測定するウェアラブルデバイス(汗乳酸センサ)の開発に着手しています(図3)。乳酸は通常体内エネルギー代謝が好気性代謝から嫌気性代謝に切り替わり解糖系にて糖からエネルギーを取り出す際に産生される物質で、直接的に嫌気性代謝閾値を示します。徐々に負荷量が増加していく運動中では、汗中乳酸値は発汗の開始後、乳酸が表皮から放出され、本センサによって選択的に検出されます。その後、運動の中盤以降で、汗の乳酸値の急激な上昇が観察され、症候限界の運動終了まで連続的に増加しました。健常者全員と汗中乳酸が測定できた14例患者において、本デバイスを用いた汗乳酸値から算出した乳酸性作業閾値が簡単に算出できました。汗乳酸性作業閾値と血中乳酸値から求めた乳酸性作業閾値を比較すると、両者は強い相関を認め(r=0.92)、Blant-altman解析でも両閾値に誤差は認めませんでした7。
我々の開発した汗乳酸センサは、皮膚に乳酸センサを貼付するだけで、運動中の汗中の乳酸値をリアルタイムかつ連続的に測定することが可能でした。また、そこから算出された乳酸性作業閾値は、血中乳酸から求めたものと一致しており、今後本デバイスから算出した乳酸性作業閾値を用いた心臓リハビリテーションに応用できる可能性があります。2022年には心疾患患者を対象に医師主導治験(治験実施計画書番号:LacS-001; jRCT2032220057)を行い、有効性の評価である主要評価項目を達成し、2024年にScientific Reports誌に掲載されました8。本治験は、株式会社グレースイメージングと共同して行いました。引き続き、当機器の医療機器製造販売承認を目指し開発を進めてまいります。これらの活動は、2023年秋に、NHKWORLDで取り上げられました。
現在、我々は、新しい携帯アプリの開発および医師主導治験を行っています(治験実施計画書番号:HFExS001; jRCT2032230388)。心不全は、心臓の機能が低下して、体に十分な血液を送り出せなくなった状態で、薬などの適切な治療に加えて、運動や食事など生活習慣の改善を目指した心臓リハビリテーションを行うことが重要とされています。しかし、心臓リハビリテーションにおける外来での運動療法は、心不全患者の10%以下にしか行われていません。したがって、通常の診療で行っている通院での運動の実践とは別の方法で、患者の在宅での運動を評価・可視化し、かつ心不全の改善に有効な運動支援の方法が求められています。そこで、我々は、心不全患者の運動を支援するアプリケーションである「運動支援アプリ」を開発し、その有効性・安全性を確認するために、医師主導治験を2023年10月より開始しました。患者がFitbitスマートウォッチを常時装着して、そこから歩数や脈拍数などの運動の状況の情報を「運動支援アプリ」が取得し、体重や生活の質のアンケート情報と合わせて、本人に最適な運動を支援するアプリケーションとなります。今回の治験によって、医療機器としての「運動支援アプリ」の承認に向けた開発を加速させます。現在、心不全患者の90%以上に、保険医療に即した適切な運動療法を届けられていない状況です。新しい医療機器を開発することで、そのような心不全患者がより豊かな生活を送れるような社会の実現が期待されます。
心血管疾患患者は、日々の体調に合わせて、適切な運動の強さで運動を行うことが重要です。特に過負荷な活動で心不全入院を繰り返すこともあり、運動による身体の負荷(疲労度)をモニターする機器を開発し、安全で効果的な運動が行えるよう支援したいと考えています。
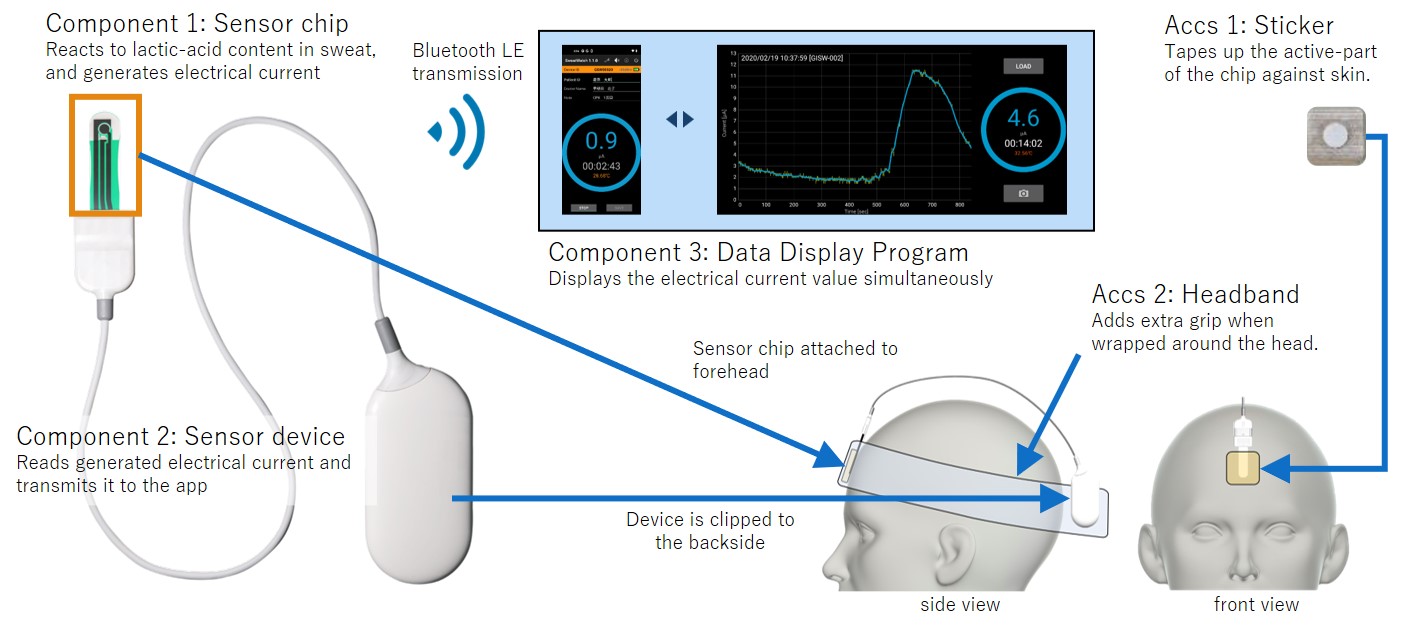
図3
関連論文
7. Seki Y, Yoshinori Katsumata, et al. A novel device for detecting anaerobic threshold using sweat lactate during exercise. Sci Rep. 2021 Mar 2;11(1):4929. doi: 10.1038/s41598-021-84381-9.リンク1 、リンク2
8.Katsumata Y *, Muramoto Y, Ishida N, Takemura R, Nagashima K, Ikoma T, Kawamatsu N, Araki M, Goda A, Okawara H, Sawada T, Ichihara YK, Hattori O, Yamaoka K, Seki Y, Ryuzaki T, Ikura H, Nakashima D, Nagura T, Nakamura M, Sato K, Shiraishi Y. Sweat lactate sensor for detecting anaerobic threshold in heart failure: a prospective clinical trial (LacS-001). Sci Rep. 2024 Aug 16;14(1):18985. doi: 10.1038/s41598-024-70001-9.
主な研究
生体センサを用いた生体情報の性能評価に関する研究開発に対するご協力のお願い(令和2年4月27日~)患者さん、健常な方、低酸素環境の協力者用、電気的筋刺激装置を用いたトレーニングを用いた研究に参加される方
非侵襲的なバイタルデータを用いたストレス・ウェルビーイング評価に関する研究開発に対するご協力のお願い(令和2年10月29日~)
「慢性疾患患者の在宅日常生活におけるバイタルデータや活動量の収集による重症化予防等への有効性の検証」の研究に対するご協力のお願い(令和1年6月25日~)
「汗乳酸センサを用いた低酸素下での最適なトレーニング強度決定手法の開発の研究(UMIN000048809)」に対するご協力のお願い(令和4年8月23日~) 、リンク2 UMIN000048809はこちら
③画期的なセンシングデバイスの開発:汗乳酸センサのスポーツへの応用
汗乳酸センサは、一般の方のみならずアスリートのトレーニングに応用できます。汗乳酸センサを用いて、一般の方やスポーツ選手にとって、トレーニングを行うのに最適な運動負荷のトレーニングの提供が可能になったことを2023年にscientific reportsに報告しました9。また、低酸素環境下や水泳中でも、汗乳酸センサの活用で、ATの有用な推定値を決定できることを報告しました(図4)1011。さらに、有酸素運動中には呼気のエアロゾルが増加しないこと、無酸素運動では増加する呼気からのエアロゾルが層流換気装置内では完全に消失することを、この汗乳酸センサを用いて証明し、2021年にpros one誌に報告しました12。有酸素運動は、COVID-19などの流行性感染症拡大を引き起こすことなく行える運動であるといえます6。現在、スポーツ医学総合センターと循環器内科が共同で以下の臨床研究を行い、多くの研究を進めています13-27。
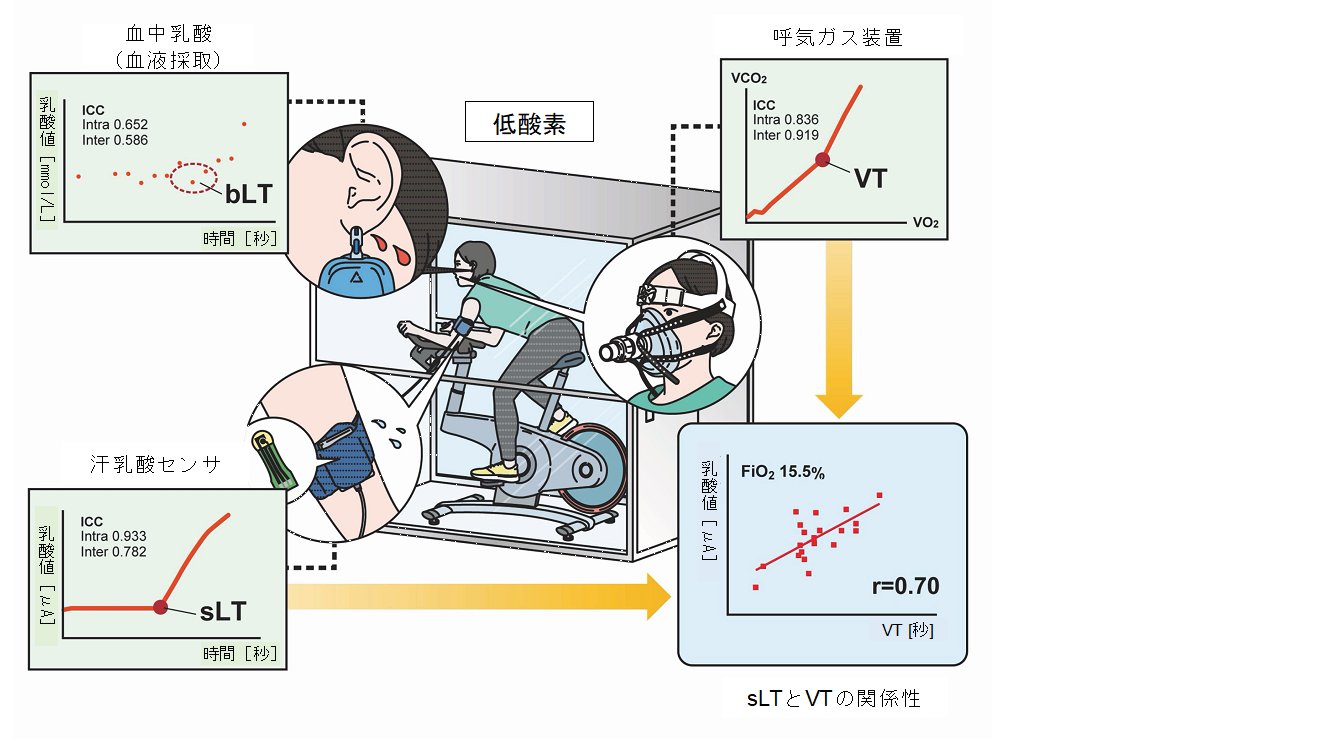
図4
発表論文
9.Muramoto Y, Nakashima D, Amano T, Harita T, Sugai K, Daigo K, Iwasawa Y, Ichihara G, Okawara H, Sawada T, Kinoda A, Yamada Y, Kimura T, Sato K, Katsumata Y. Estimation of maximal lactate steady state using the sweat lactate sensor. Sci Rep. 2023 Jun 26;13(1):10366. doi: 10.1038/s41598-023-36983-8.
10.Okawara H, Iwasawa Y, Sawada T, Sugai K, Daigo K, Seki Y, Ichihara G, Nakashima D, Sano M, Nakamura M, Sato K, Fukuda K, Katsumata Y. Anaerobic threshold using sweat lactate sensor under hypoxia. Sci Rep. 2023 Dec 21;13(1):22865. doi: 10.1038/s41598-023-49369-7.
11.Okawara H, Sawada T, Nakashima D, Fujitsuka H, Muramoto Y, Hinokuma D, Oshikiri Y, Ishizaki K, Miki J, Hara R, Sano M, Sato K, Nakamura M, Nagura T, Katsumata Y *. Lactate threshold evaluation in swimming using a sweat lactate sensor: A prospective study. Eur J Sport Sci. 2024 Sep;24(9):1302-1312. doi:10.1002/ejsc.12179.
12.Katsumata Y, et al. Laminar flow ventilation system to prevent airborne infection during exercise in the COVID-19 crisis: A single-center observational study. PLoS One, 2021 Nov 10;16(11):e0257549. doi: 10.1371/journal.pone.0257549.
13.Maeda Y, Okawara H, Sawada T, Nakashima D, Nagahara J, Fujitsuka H, Ikeda K, Hoshino S, Kobari Y, Katsumata Y, Nakamura M, Nagura T. Implications of the Onset of Sweating on the Sweat Lactate Threshold. Sensors (Basel). 2023 Mar 23;23(7):3378. doi: 10.3390/s23073378.
14. Daigo K, Katsumata Y, Esaki K, Iwasawa Y, Ichihara G, Miura K, Shirakawa K, Sato Y, Sato K, Fukuda K. Predictors of Improvement in Exercise Tolerance After Balloon Pulmonary Angioplasty for Chronic Thromboembolic Pulmonary Hypertension. J Am Heart Assoc. 2023 Feb 7;12(3):e8137. doi: 10.1161/JAHA.122.027395.
15.Sawada T, Okawara H, Nakashima D, Ikeda K, Nagahara J, Fujitsuka H, Hoshino S, Maeda Y, Katsumata Y, Nakamura M, Nagura T. Constant Load Pedaling Exercise Combined with Electrical Muscle Stimulation Leads to an Early Increase in Sweat Lactate Levels. Sensors (Basel). 2022 Dec 7;22(24):9585. doi: 10.3390/s22249585.
16.Sawada T, Katsumata Y, et al. Constant Load Pedaling Exercise Combined with Electrical Muscle Stimulation Leads to an Early Increase in Sweat Lactate Levels. Sensors (Basel). 2022 Dec 7;22(24):9585. doi: 10.3390/s22249585.
17.Okawara H, Katsumata Y, et al. Realtime Monitoring of Local Sweat Rate Kinetics during Constant-Load Exercise Using Perspiration-Meter with Airflow Compensation System. Sensors (Basel). 2022 Jul 22;22(15):5473. doi:10.3390/s22155473.
18.Okawara H, Katsumata Y, et al. Kinetic changes in sweat lactate following fatigue during constant workload exercise. Physiol Rep. 2022 Jan;10(2):e15169. doi: 10.14814/phy2.15169.
19.Kimura T, Mącznik A, Kinoda A, Yamada Y, Muramoto Y, Katsumata Y, Sato K. Prevalence and Factors Associated with Mental Health Complaints in Japanese Collegiate Athletes. Sports (Basel). 2024 Sep 2;12(9):240. doi: 10.3390/sports12090240. PMID: 39330717; PMCID: PMC11435743.
20.Kinoda A, Mącznik A, Kimura T, Muramoto Y, Katsumata Y, Sato K. 1-Year Prevalence and Factors Related to Injuries and Illnesses in Japanese Judo Collegiate Athletes. J Funct Morphol Kinesiol. 2024 Aug 28;9(3):148. doi: 10.3390/jfmk9030148
21.Muramoto Y, Kimura T, Kinoda A, Yamada Y, Katsumata Y *, Sato K. Web-based survey on injuries among ultimate frisbee athletes in Japanese college sports:sex differences in injury location and onset. BMC Sports Sci Med Rehabil. 2024 Aug 22;16(1):175. doi: 10.1186/s13102-024-00964-9.
22.Sawada T, Okawara H, Nakashima D, Aoki K, Namba M, Iwabuchi S, Katsumata Y, Nakamura M, Nagura T. Local alternating heat and cold stimulation affects hemodynamics and oxygenation in fatigued muscle tissue and autonomic nervous activity: a single-arm interventional study. J Physiol Anthropol. 2024 Mar 25;43(1):11. doi: 10.1186/s40101-024-00358-3.
23.Kimura T, Mącznik AK, Kinoda A, Yamada Y, Muramoto Y, Katsumata Y, Sato K. Injury prevalence and associated factors among Japanese lacrosse collegiate athletes. Front Sports Act Living. 2024 Mar 5;6:1360639. doi:10.3389/fspor.2024.1360639.
24.関 雄太、中島 大輔、勝俣 良紀、汗乳酸センサを用いた運動負荷試験の可能性、BioClinica 37 (3). 2022 (249) 31-35
25.勝俣 良紀、中島 大輔、新しいバイオセンサを活用した心臓リハビリテーション、医学書院『循環器ジャーナル』2023
26.勝俣 良紀、中島 大輔、汗乳酸ウェアラブルデバイスによる運動負荷測定の意義とデジタル医療での応用、メジカルビュー社 Heart View 2023
④低酸素環境での運動の有効性
低酸素トレーニングは、アスリートのトレーニング方法として活用されている。低酸素環境での運動は、一般的には、常酸素環境と比較して、運動レベルが低下するが、一部のアスリートでは、低酸素環境でも運動レベルが変わらないことがある。その原因は、それまでのトレーニング方法なども1つの原因と考えられているが、本人の体質(低酸素環境に耐性をもっているかどうか)も関与していることが考えられます。そこで、この研究では、22名の大学生の自転車競技のアスリートを対象に、低酸素環境での運動能力が落ちるか変わらないかの原因となる遺伝的関与を評価することを目的としました。具体的には、通常の酸素濃度(20.9%)および低酸素環境(15.5%:標高2500m相当)における症候限界までの漸増負荷試験を無作為クロスオーバー法(どちらの酸素濃度を先行して行うかをランダムに振り分けました)で実施し、運動に関連する多くの遺伝子型で低酸素運動中の最大酸素摂取量(Peak VO2)と血中乳酸の蓄積にどのように影響するかを評価しました。その結果、ACE-II遺伝子型を有する選手は、血中乳酸の上昇速度が遅く、最大運動時の血中乳酸値も低いことがわかりました。また、低酸素環境下で運動では、最大酸素摂取量:PeakVO2(運動能力)が低下しやすいことがわかりました27。低酸素トレーニングの効果を最大限に引き出すために、個々人の遺伝的特徴に基づいたトレーニングプログラムの開発が望まれます。特に持久力向上を目指すアスリートにとって、ACE遺伝子の分析を組み込んだトレーニングは、新たなトレーニング戦略の一つとして期待されています。
現在、動物実験やヒトを対象とした研究を進め、低酸素運動に関する疾患や健康への影響について、メカニズムを含めて検証を進めている。
発表論文
27.Muramoto Y, Momoi M, Nakashima D, Omae K, Sugai K, Daigo K, Iwasawa Y, Ichihara G, Okawara H, Sawada T, Kinoda A, Yamada Y, Kimura T, Sato K, Katsumata Y. Angiotensin-converting gene and hypoxic exercise tolerance: a randomized crossover trial. Int J Sports Med. 2025 Jan 9. doi: 10.1055/a-2477-0512.
⑤リアルタイム心拍変動解析システムを用いた、健康管理
これまで、心拍変動がうつや不安、ストレス、Well-beingと関連していることは報告されているが、計測機器・手法および解析手法などの点から自身で簡易的に計測した心拍変動値*1の妥当性を考慮した応用は実現できていませんでした。また心拍変動結果の解釈についても、一般的な基準値をその判定に用いられていた点も問題であり、従来から行われている、単回の心拍変動の結果を用いた、うつや不安、ストレス、Well-beingの予測はその精度が課題でした。加えて、労働生産性の指標となるプレゼンティーイズム*2との関連に関しては、十分に解析が進んでいません。上記の課題に対して、市販されているスマートウォッチを用いて、より簡易的・即時的な心拍変動計測・解析手法を開発し、日々の計測に応用することで不安・労働生産性を評価する試みを日清食品ホールディングス株式会社との共同研究として実施しました。健常なオフィスワーカーを対象にApple Watchを用いて、2ヵ月間、毎朝30秒の心拍変動解析データを収集するとともに、不安状態を定量化するためにSTAI(State-Trait Anxiety Inventory)*3のアンケートに回答してもらいました。また、プレゼンティーイズムの定量化のため、Work Limitation Questionnaire(WLQ)*4にも回答してもらいました。その結果、HRVを30日以上モニターした279名(男性比率83.9%、年齢42±10歳)のHRVデータが収集され、HRV解析で求められる、HF(高周波成分)及び、LF(低周波成分)とHFの比であるL/Hの対数変換値(LnccvHF、Lnccv L/H)は、特性不安(不安に対する感度)が高い性質を持つ群で低い群と比較して、高い分散を示しました。さらに、これらの予測モデルを利用して高特性不安を予測する適切なカットオフに基づき、連日の心拍変動解析の結果を2群に分けると、特性不安予測モデルのスコアが高い群においては、プレゼンティーイズムの指標であるWLQ生産性低下スコアが高い値を示すことがわかりました(p = 0.02、r = 0.17)。日々計測したHRVの分散状態に着目することで、簡易的かつ即時的に、不安と労働生産性の定量的モニタリングが期待されます28。
発表論文
本研究に従事している関係者
慶應義塾大学循環器内科
白石泰之
慶應義塾大学スポーツ医学総合センター
勝俣良紀、村本勇貴
慶應義塾大学整形外科
大川原洋樹、澤田智紀
共同研究機関
慶應義塾大学、岐阜大学、株式会社グレースイメージング、株式会社シグマテクノロジー
研究費
1. 平成28年度 福田記念医療技術振興財団研究助成事業、助成テーマ「心臓自律神経反射機能の画像診断技術による非監視下運動療法への応用研究」
2. 平成29年度 日本心臓リハビリテーション学会学術研究助成、「心臓自律神経反射機能リアルタイム画像を用いた自動有酸素運動通知システムおよび新規運 動療法の開発」
3. 平成30年度 武田薬品工業株式会社Takeda Japan Medical Affairs Funded Research Grant 2018、「リアルタイム心拍変動解析と運動強度の自己管理システムの開発」
4. 平成30年度 明治安田厚生事業団 体力医学研究所 第35回若手研究者のための健康科学研究助成、「心血管疾患予防に向けた、リアルタイム心拍変動解析と運動強度の自己管理システムの開発」
5. 第31回(2019年度) 中冨健康科学振興財団研究助成金、「心血管疾患予防に向けた、リアルタイム心拍変動解析と運動強度の自己管理システムの開発」
6. 第41回(2019年度) 公益財団法人石本記念デサントスポ―ツ科学振興財団学術研究、「心血管疾患予防に向けた、リアルタイム心拍変動解析と運動強度の自己管理システムの開発」
7. 令和1年度 日本医療研究開発機構(AMED)循環器疾患・糖尿病等生活習慣病対策実用化研究事業、助成テーマ「心血管疾患に対する、乳酸測定ウェアラブルデバイスを用いた運動強度の自己管理システムの開発」
8. 第39回(令和元年度) 木村記念循環器財団研究助成、助成テーマ「心血管疾患予防に向けた、生体バイオセンサを用いた運動強度の自己管理システムの開発
9. 令和1年度 公益財団法人鈴木謙三記念医科学応用研究財団令和元年度調査研究助成、助成テーマ「心血管疾患予防に向けた、生体バイオセンサを用いた運動強度の自己管理システムの開発」
10. 2019年度 公益財団法人 総合健康推進財団第36回一般研究奨励助成助成テーマ「心血管疾患予防に向けた、生体バイオセンサを用いた運動強度の自己管理システムの開発」
11. 2020年度 パブリックヘルス科学研究助成金、助成テーマ「心血管疾患予防に向けた、生体バイオセンサを用いた運動強度の自己管理システムの開発」
12. 2020年度 IoT健康ライフ研究コンソーシアム プロジェクト(慶應義塾大学 グローバルリサーチインスティテュート)、助成テーマ「リアルタイム心拍変動解析を用いた、ストレス状態および運動量の「見える化」と行動変容プログラムの開発」
13. 2020年度 テルモ生命科学振興財団研究開発助成、助成テーマ「乳酸センサを用いた乳酸値連続測定の遠隔モニタリング技術の開発」
14. 2021年度 国立研究開発法人 科学技術振興機構 共創の場形成支援プログラム(COI-NEXT)、分担、助成テーマ「誰もが参加し繋がることで、ウェルビーイングを実現する都市型ヘルスコモンズ共創拠点」
15. 2022年度 AMED循環器疾患・糖尿病等生活習慣病対策実用化研究事業、代表、助成テーマ「心血管疾患に対する、運動支援プログラムに関する研究開発」
16. 令和4年度 日本心臓リハビリテーション学会学術研究助成 代表、「心不全に対する、身体活動支援プログラムに関する研究開発」
17. 2022年度(第49回)大和証券ヘルス財団調査研究助成 代表、「心血管疾患に対する、運動支援プログラムに関する研究開発」